Резюме
Главная
Методы
Вирусы, клетки, инфекции in vitro и анализы бляшек.
Кластеризация последовательностей и структурное моделирование.
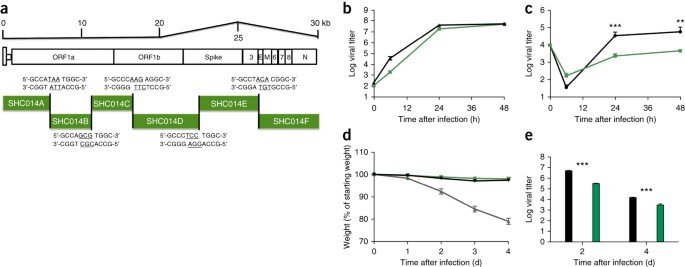
Конструирование химерных вирусов, подобных SARS.
Этическое заявление.
Мыши и инфекция in vivo.
Гистологический анализ.
Анализы на нейтрализацию вирусов.
Статистический анализ.
Биобезопасность и биозащита.
Коды присоединения
История изменений
30 марта 2020 года Примечание редакции, март 2020 года: мы знаем, что эта статья используется в качестве основы для непроверенных теорий о том, что новый коронавирус, вызывающий COVID-19, был спроектирован. Нет никаких доказательств того, что это правда; ученые считают, что животное является наиболее вероятным источником коронавируса. 20 ноября 2015 года В версии этой статьи, первоначально опубликованной в интернете, авторы не признали источник финансирования, USAID-EPT-PREDICT funding from EcoHealth Alliance, до Z.-L. S. ошибка была исправлена для печатных, PDF и HTML версий этой статьи.
Рекомендации
- 1
Ge, X. Y. et al. Выделение и характеристика атипичного коронавируса летучей мыши, использующего рецептор ACE2. Nature 503 , 535-538 (2013). - 2
Yount, B. et al. Обратная генетика с полноразмерной инфекционной кднк коронавируса тяжелого острого респираторного синдрома. Прок. Натл. Acad. Sci. USA 100 , 12995-13000 (2003). - 3
Беккер, М. М. и др. Синтетический рекомбинантный коронавирус летучей мыши, подобный SARS, заразен в культивируемых клетках и у мышей. Proc. Натл. Acad. Sci. USA 105 , 19944-19949 (2008). - 4
Peiris, J. S., Guan, Y. & Yuen, K. Y. тяжелый острый респираторный синдром. Nat. Med. 10 , S88–S97 (2004). - 5
Аль-Тауфик, Дж.А. и др. Эпиднадзор за возникающими респираторными вирусами. Ланцет-Инфекция. Дис. 14 , 992-1000 (2014). - 6
Он, Б. и др. Идентификация различных альфакоронавирусов и геномная характеристика нового тяжелого острого респираторного синдрома–подобного коронавируса от летучих мышей в Китае. J. Virol. 88 , 7070-7082 (2014). - 7
Ли Ф. распознавание рецепторов и межвидовые инфекции коронавируса атипичной пневмонии. Antiviral Res . 100 , 246-254 (2013). - 8
Sheahan, T. et al. Механизмы распространения зоонозного тяжелого острого респираторного синдрома коронавируса хозяина в эпителии дыхательных путей человека. J. Virol. 82 , 2274-2285 (2008). - 9
Есикава, Т. и др. Динамические врожденные иммунные реакции клеток бронхиального эпителия человека на тяжелую коронавирусную инфекцию, ассоциированную с острым респираторным синдромом. PLoS ONE 5 , e8729 (2010). - 10
Qiu, X. et al. Реверсия прогрессирующей болезни , вызванной вирусом Эбола, у нечеловеческих приматов с помощью ZMapp. Nature 514 , 47-53 (2014). - 11
Sui, J. et al. Расширение нейтрализующей активности для прямого блокирования доминирующего антитело-управляемого пути эволюции атипичной пневмонии-коронавируса. PLoS Pathog. 4 , e1000197 (2008). - 12
Sui, J. et al. Влияние антител к человеческому анти–спайковому белковому рецептору, связывающему домен, на нейтрализацию коронавируса тяжелого острого респираторного синдрома и физическую форму. J. Virol. 88 , 13769-13780 (2014). - 13
Rockx, B. et al. Escape from human monoclonal antibody neutralization affects in vitro and in vivo fitness of severe acute respiratory syndrome coronavirus. J. Infect. Dis. 201, 946–955 (2010).
- 14
Spruth, M. et al. A double-inactivated whole-virus candidate SARS coronavirus vaccine stimulates neutralizing and protective antibody responses. Vaccine 24, 652–661 (2006).
- 15
Bolles, M. et al. A double-inactivated severe acute respiratory syndrome coronavirus vaccine provides incomplete protection in mice and induces increased eosinophilic proinflammatory pulmonary response upon challenge. J. Virol. 85, 12201–12215 (2011).
- 16
Siegrist, C.-A. in Vaccines 6th edn. (eds. Plotkin, S.A., Orenstein, W.A. & Offit, P.A.) 14–32 (W.B. Saunders, 2013).
- 17
Deming, D. et al. Vaccine efficacy in senescent mice challenged with recombinant SARS-CoV bearing epidemic and zoonotic spike variants. PLoS Med. 3, e525 (2006).
- 18
Graham, R.L., Donaldson, E.F. & Baric, R.S. A decade after SARS: strategies for controlling emerging coronaviruses. Nat. Rev. Microbiol. 11, 836–848 (2013).
- 19
Graham, R.L. & Baric, R.S. Recombination, reservoirs and the modular spike: mechanisms of coronavirus cross-species transmission. J. Virol. 84, 3134–3146 (2010).
- 20
Agnihothram, S. et al. A mouse model for betacoronavirus subgroup 2c using a bat coronavirus strain HKU5 variant. MBio 5, e00047-14 (2014).
- 21
Relman, D.A. Metagenomics, infectious disease diagnostics and outbreak investigations: sequence first, ask questions later? J. Am. Med. Assoc. 309, 1531–1532 (2013).
- 22
Kaiser, J. Moratorium on risky virology studies leaves work at 14 institutions in limbo. ScienceInsider http://news.sciencemag.org/biology/2014/11/moratorium-risky-virology-studies-leaves-work-14-institutions-limbo (2014).
- 23
Frieman, M. et al. Molecular determinants of severe acute respiratory syndrome coronavirus pathogenesis and virulence in young and aged mouse models of human disease. J. Virol. 86, 884–897 (2012).
- 24
Ren, W. et al. Difference in receptor usage between severe acute respiratory syndrome (SARS) coronavirus and SARS-like coronavirus of bat origin. J. Virol. 82, 1899–1907 (2008).
- 25
Sims, A.C. et al. Release of severe acute respiratory syndrome coronavirus nuclear import block enhances host transcription in human lung cells. J. Virol. 87, 3885–3902 (2013).
- 26
Fulcher, M.L., Gabriel, S., Burns, K.A., Yankaskas, J.R. & Randell, S.H. Well-differentiated human airway epithelial cell cultures. Methods Mol. Med. 107, 183–206 (2005).
- 27
Roberts, A. et al. A mouse-adapted SARS-coronavirus causes disease and mortality in BALB/c mice. PLoS Pathog. 3, e5.
Acknowledgements
Research in this manuscript was supported by grants from the National Institute of Allergy & Infectious Disease and the National Institute of Aging of the US National Institutes of Health (NIH) under awards U19AI109761 (R.S.B.), U19AI107810 (R.S.B.), AI085524 (W.A.M.), F32AI102561 (V.D.M.) and K99AG049092 (V.D.M.), and by the National Natural Science Foundation of China awards 81290341 (Z.-L.S.) and 31470260 (X.-Y.G.), and by USAID-EPT-PREDICT funding from EcoHealth Alliance (Z.-L.S.). Human airway epithelial cultures were supported by the National Institute of Diabetes and Digestive and Kidney Disease of the NIH under award NIH DK065988 (S.H.R.). We also thank M.T. Ferris (Dept. of Genetics, University of North Carolina) for the reviewing of statistical approaches and C.T. Tseng (Dept. of Microbiology and Immunology, University of Texas Medical Branch) for providing Calu-3 cells. Experiments with the full-length and chimeric SHC014 recombinant viruses were initiated and performed before the GOF research funding pause and have since been reviewed and approved for continued study by the NIH. The content is solely the responsibility of the authors and does not necessarily represent the official views of the NIH.
Author information
Affiliations
Contributions
V.D.M. designed, coordinated and performed experiments, completed analysis and wrote the manuscript. B.L.Y. designed the infectious clone and recovered chimeric viruses; S.A. completed neutralization assays; L.E.G. helped perform mouse experiments; T.S. and J.A.P. completed mouse experiments and plaque assays; X.-Y.G. performed pseudotyping experiments; K.D. generated structural figures and predictions; E.F.D. generated phylogenetic analysis; R.L.G. completed RNA analysis; S.H.R. provided primary HAE cultures; A.L. and W.A.M. provided critical monoclonal antibody reagents; and Z.-L.S. provided SHC014 spike sequences and plasmids. R.S.B. designed experiments and wrote manuscript.
Corresponding authors
Ethics declarations
Competing interests
The authors declare no competing financial interests.
Supplementary information
Supplementary Text and Figures
Supplementary Figures 1–6 and Supplementary Tables 1–4 (PDF 4747 kb)
Rights and permissions
About this article
Cite this article
Menachery, V., Yount, B., Debbink, K. et al. A SARS-like cluster of circulating bat coronaviruses shows potential for human emergence. Nat Med 21, 1508–1513 (2015). https://doi.org/10.1038/nm.3985
Received:
Accepted:
Published:
Issue Date:
Further reading
-
Decoding Covid-19 with the SARS-CoV-2 Genome
Current Genetic Medicine Reports (2021)
-
In silico T cell epitope identification for SARS-CoV-2: Progress and perspectives
Advanced Drug Delivery Reviews (2021)
-
TSP-based PCR for rapid identification of L and S type strains of SARS-CoV-2
Indian Journal of Medical Microbiology (2021)
-
Tracing the origins of SARS-COV-2 in coronavirus phylogenies: a review
Environmental Chemistry Letters (2021)
-
Gebelik, Dogum ve Dogum Sonu Donemde COVID-19 Enfeksiyonu ve Yonetimi
Kocaeli Universitesi Sagl?k Bilimleri Dergisi (2021)